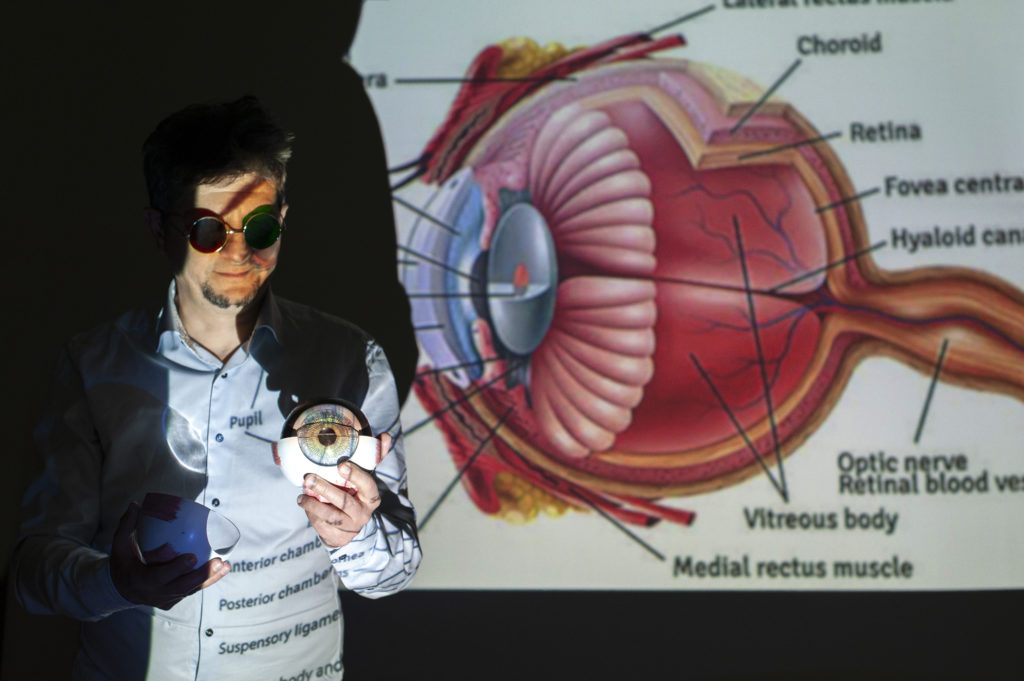
Na świecie na poważne zaburzenia wzroku lub ślepotę cierpi aż 285 milionów ludzi. Niestety, większość z nich nie ma dostępu do nowoczesnych metod leczenia, przez co na pomoc często przychodzi za późno. Może się to zmienić dzięki usprawnieniu narzędzia diagnostycznego do wykrywania patologii oka znanego od trzech dekad.
Tomografia optyczna OCT jest jednym z najbardziej podstawowych i najdokładniejszych badań wykorzystywanych w diagnostyce chorób oczu. Pozwala szczegółowo obejrzeć poszczególne struktury oczu, a tym samym wykryć choroby plamki żółtej, zmiany cukrzycowe siatkówki, jaskrę czy nowotwory. Niestety, nie jest to metoda idealna, bo naturalnie pojawiające się szumy podczas badania znacznie ograniczają dokładność obrazowania. Zespół naukowców z Międzynarodowego Centrum Badań Oka (ICTER) postanowił to zmienić, wprowadzając do metody OCT istotne zmiany. Tak powstała jeszcze lepsza czasowo-częstotliwościowa tomografia optyczna OCT, która tłumi szumy i pozwala na uzyskiwanie dokładnych obrazów.
Badania zostały przeprowadzone przez dr Edgidijusa Auksoriusa, dr Dawida Boryckiego, Piotra Węgrzyna i prof. Macieja Wojtkowskiego z ICTER, a wyniki opublikowano w czasopiśmie „Optics Letters” w pracy zatytułowanej „Multimode fiber as a tool to reduce cross talk in Fourier-domain full-field optical coherence tomography„.
Jak przebiega badanie OCT?
Metodę OCT cechuje wysoka rozdzielczość, dlatego jest jednym z najczęściej stosowanych badań okulistycznych. Jest całkowicie bezbolesna i bezpieczna – nie ma żadnych przeciwwskazań do jej stosowania (badanie może być wykonywane nawet u kobiet w ciąży). Najlepiej sprawdza się w diagnostyce oczu, np. postępu jaskry, retinopatii cukrzycowej, czy zwyrodnienia plamki żółtej związanego z wiekiem (AMD), które stanowią najczęstszą przyczynę utraty widzenia centralnego wśród osób w podeszłym wieku. W początkowej fazie AMD na dnie oka można zaobserwować pojedyncze złogi, czyli przegrupowania barwnika oraz subtelne zmiany zanikowe. Podczas gdy w przypadku rozwoju cukrzycy w obrazach OCT obserwuje się zmiany struktury mikronaczyniowej siatkówki.
Samo badanie OCT trwa kilka-kilkanaście minut. Pacjent siada przed specjalnym aparatem i ma patrzeć we wskazany przez lekarza punkt, ograniczając mruganie. Głowica pomiarowa ustawiona jest 2-3 cm od oka, więc nie ma możliwości, by miała jakikolwiek kontakt z naszym narządem wzroku. W większości przypadków badanie OCT nie wymaga specjalnego przygotowania – pacjent może przyjechać na nie samochodem. Sama interpretacja wyników jest jednak złożona, dlatego powinna być przeprowadzona przez doświadczonego okulistę.
Biofizyka OCT
Zrozumienie podstaw fizycznych badania OCT nie jest łatwe. Technika ta pozwala na przeprowadzenie „biopsji optycznej” w czasie rzeczywistym, czyli wizualizacje mikrostruktury tkanki oraz zdiagnozowanie ewentualnych zmian patologicznych. W tomografii optycznej wszelkie dane o strukturze obiektu są uzyskiwane z natężenia sygnału interferencyjnego (powstałego w wyniku nakładania się dwóch wiązek laserowych). Tomografia optyczna OCT stosowana obecnie w gabinetach okulistycznych na całym świecie wykorzystuje ciekawą własność światła, zwaną spójnością w czasie lub spójnością w przestrzeni. Podczas badania OCT wykorzystuje się źródła światła częściowo spójnego (czasowo, ale nie przestrzennie) – aparat dokonuje pomiaru różnicy dróg optycznych między zwierciadłem w interferometrze a kolejnymi warstwami próbki obiektu (okiem).
Wewnątrz interferometru znajduje się specjalna płytka, która dzieli promienie na dwie części i rejestruje interferencję promienia odbitego od struktur tkanek i promienia padającego. Znając różnice dróg optycznych, można określić położenie analizowanych struktur oka. Dane są przetwarzane przez komputer, a następnie prezentowane pod postacią dwuwymiarowych obrazów przekrojów (tomogramów).
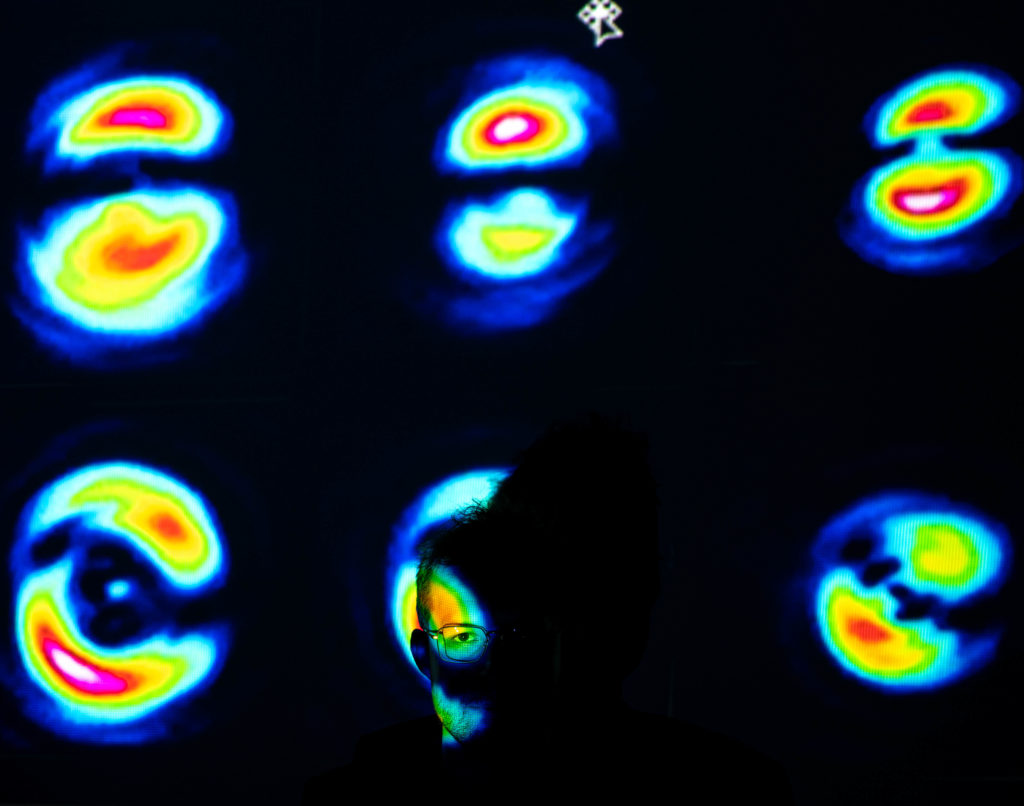
Tkanki to struktury wieloskładnikowe, które w różny sposób rozpraszają światło. W zależności od stopnia odbicia lub pochłaniania promieniowania, prezentowany jest obraz w skali szarości lub barwach. Obiekty o najwyższym współczynniku odbicia widoczne są na czerwono lub biało, a o najsłabszym sygnale w ciemnych kolorach lub ciemnoszaro. Tkanki o pośrednich wartościach odbijania światła prezentują się w barwie żółto-zielonej lub odcieniach szarości.
W przypadku tomografii optycznej z użyciem światła częściowo spójnego wykorzystywana jest interferometria niskokoherentna, czyli taka, w której interferencja promieniowania zachodzi na drodze rzędu mikrometrów (dzięki zastosowaniu diod superluminescencyjnych lub laserów o krótkich impulsach). Zazwyczaj stosuje się źródła promieniowania z zakresu podczerwieni. Do klasycznego badania OCT nie można stosować źródeł światła niespójnego (np. halogenów, LED-ów czy żarówek).
Zespół naukowców z Międzynarodowego Centrum Badań Oka (ICTER) jako pierwszy na świecie połączył właściwości spójności światła w czasie i przestrzeni, co umożliwia dokładniejszą diagnostykę oka.
Jak można usprawnić metodę OCT?
Czasowo-częstotliwościowa tomografia optyczna OCT (Spatio-Temporal Optical Coherence Tomography STOC-T) jest skutecznym narzędziem do obrazowania oka dzięki swojej szybkości i zdolności do pozyskiwania stabilnej informacji fazowej w pełnym polu widzenia (nie dla skanującej, skupionej wiązki jak w przypadku lasera). Do tej pory, głównym problemem przy stosowaniu tej metody (od 2006 r.), był szum (tzw. plamki), który utrudnia dokładną wizualizację naczyniówki – części oka kluczowej ze względu na udział w patogenezie wielu chorób (dostarcza tlen i składniki odżywcze do fotoreceptorów). Naukowcy z ICTER wykoncypowali, że użycie światłowodu wielomodowego o odpowiedniej długości, poprawia obrazowanie oka.
Światłowód wielomodowy to taki, który na swoim końcu emituje kilkaset niepowtarzających się wzorów przestrzennych w przekroju wiązki (tzw. modów poprzecznych). Do tej pory wykorzystywano wielokrotnie takie urządzenia do transmisji danych za pomocą światła, ale nikt nie wpadł na to, że kilkaset metrów takiego światłowodu powoduje, że każdy ze wzorków przestrzennych będzie wychodził z niego w różnym czasie. Dzięki temu uzyskuje się kilkaset obrazów OCT rejestrowanych w tym samym pomiarze, które po dodaniu do siebie redukują niepożądane efekty, takie jak szum plamkowy. Dzięki wykorzystaniu tego pomysłu do OCT zespół uczonych z ICTER opracował nowy sposób kontroli fazy optycznej STOC-T, który pozwolił na uzyskanie in vivo obrazów siatkówki i rogówki w wysokiej rozdzielczości. Ta metoda pozwala znacznie lepiej zobaczyć obrazy przekrojów z warstwy naczyniowej znajdującej się pod siatkówką (do tej pory nie było to możliwe). Warto podkreślić, że światłowód był używany pasywnie, bez żadnych ruchomych elementów.
Tomografia optyczna OCT jest jednym z rutynowych badań okulistycznych na całym świecie. Dzięki usprawnieniom zespołu ICTER, pozwoli ona na identyfikowanie zmian na poziomie komórkowym, co przełoży się na lepszą diagnostykę oraz zrozumienie powstawania różnych chorób oczu.
Autor: Marcin Powęska
Zdjęcia Piotra Węgrzyna wykonał: Karol Karnowski

Publikacja
Tytuł:
Autorzy:
Egidijus Auksorius, Dawid Borycki, Piotr Wegrzyn, Ieva Žičkienė, Karolis Adomavičius, Bartosz L. Sikorski, and Maciej Wojtkowski.
Magazyn naukowy:
Optics Letters Vol. 47,Issue 4, pp. 838-841(2022) DOI: https://doi.org/10.1364/OL.449498